我校伟德官网下载客户端劉熠教授在藥物化學領域頂尖期刊Journal of Medicinal Chemistry(IF: 6.8)發表研究成果“An Activatable Heavy-Atom-Free Upconversion Photosensitizer for targeted Imaging and Treatment of Tumors”。團隊博士生趙超為本文的第一作者,劉熠教授、潘怡副教授和東南大學汪海燕副研究員為共同通訊作者,伟德官网下载客户端為本文第一通訊單位。
近年來,劉熠團隊在近紅外頻率上轉換光診療領域開展了大量的研究工作(Coordination Chemistry Reviews, 2025, 524, 216303; Journal of Medicinal Chemistry, 2024, 67, 22322-22331; Journal of Medicinal Chemistry, 2024, 67, 13383−13391; Acta Pharmaceutica Sinica B, 2024, 14, 378-391; Coordination Chemistry Reviews, 2023, 496, 215379; Acta Biomaterialia, 2023, 155, 554; Chemical Engineering Journal, 2022, 430, 132858)。光動力療法(PDT)是一種新型的腫瘤治療方法,具有無創性、廣譜性、良好耐受性和不良反應小等優點,已經引起了廣泛關注;但仍面臨幾個挑戰,例如缺乏選擇性、光的深層穿透力不足以及有效活性氧(ROS)的生成效率低。研究人員以半花菁染料為結構骨架,開發了一系列頻率上轉換發光的光敏劑,其中在近紅外光照射下隻有NFh-NMe-2可有效産生1O2,同時産生明顯的頻率上轉換發光信号。基于腫瘤微環境中過表達的硝基還原酶(NTR),用對硝基苄基修飾光敏劑NFh-NMe-2,獲得可激活的FUCL光敏劑NFh-NTR;NFh-NTR能夠被NTR激活,這一激活過程導緻光敏劑NFh-NMe-2的釋放和上轉換發光的開啟。在近紅外光激發下,産生大量的1O2,能夠精确地針對含有光敏劑的細胞,減少對周圍健康組織的損害。NFh-NTR通過凋亡機制誘導細胞死亡,并在體外和體内表現出良好的抗腫瘤效果。這項工作為腫瘤治療中FUCL光敏劑的化學設計開辟了新的策略。
該研究工作獲得國家自然科學基金(82272148和82073227)項目資助。
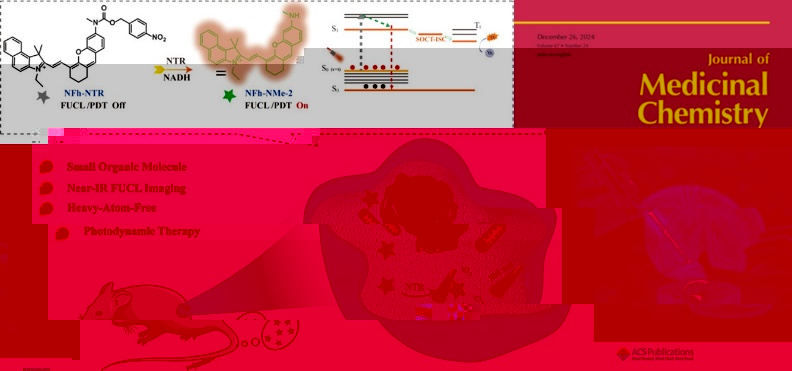
可激活型上轉換發光有機光敏劑的響應過程示意圖
文章鍊接:https://doi.org/10.1021/acs.jmedchem.4c02679
(供稿單位:伟德官网下载客户端生物醫學工程與診斷藥學系,撰寫人:于慧)

